深圳先进院团队等发现金黄色葡萄球菌反复感染的新机制
近日,中国科学院深圳先进技术研究院合成所黄建东团队与香港大学医学院等单位合作完成的最新研究成果以Adenosine synthase A contributes to recurrent Staphylococcus aureus infection by dampening protective immunity为题在柳叶刀旗下的EBioMedicine(IF 8.143)上发表。该研究发现了腺苷合成酶A可以通过抑制保护性Th1/Th17的免疫反应而导致金黄色葡萄球菌(金葡菌)的反复感染。深圳先进院合成所张宝中副研究员、香港大学生物医学学院邓健博士和微生物系朱轩博士为该论文的共同第一作者。深圳先进院客座研究员黄建东和袁国勇院士为共同通讯作者。
金葡菌是导致医院和社区严重感染的最常见病原体之一。可以引起不同程度的疾病,从轻微的皮肤或黏膜感染到甚至危及生命的脓毒血症、败血症或肺炎等。它已成为全球重症监护病房(ICU)、创伤等感染率最高的病原菌,也是最为常见的耐药菌之一。耐甲氧西林金葡菌(MRSA)的出现严重威胁了公共卫生安全。
值得引起注意的是,之前感染过金葡菌并不足以建立保护性免疫并预防随后的感染,这种情况在复发性皮肤和软组织感染中尤为明显。金葡菌感染后宿主不能建立起保护性免疫,相关机制尚不明确,这导致对其疫苗的研发比较缓慢。
目前,已经确定了几种宿主因素与抗金葡菌感染的作用有关:补体系统、中性粒细胞、γδ+ T细胞产生的IL-17、B细胞免疫应答、Th1和Th17免疫应答等。其中,越来越多的证据表明细胞免疫与金葡菌的反复感染密切相关。然而,在病原体与宿主的军备竞赛中,金葡菌已经进化出多种策略来压制宿主的获得性免疫力的建立。葡萄球菌蛋白A(SpA)是一种明确的致病因子,能够通过增强B细胞超抗原活性并阻断抗体介导的吞噬作用来干扰B细胞活力和功能。到目前为止,只有肽聚糖O-乙酰基转移酶(OatA)被证明可以通过阻断NLRP3炎性小体信号通路,进而直接影响Th17保护性细胞免疫反应的建立。所以,探究金葡菌逃避宿主保护性免疫反应的潜在机制,对于金葡菌疫苗的开发具有重要的意义。
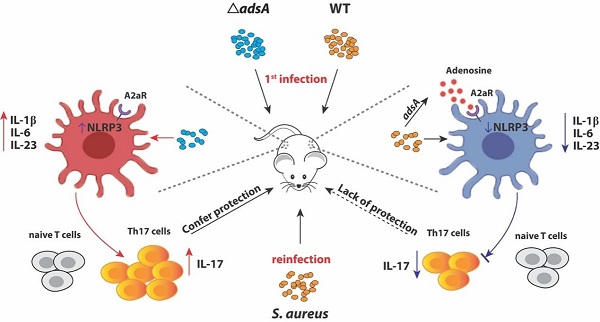
该研究提供证据表明,金葡菌细胞壁锚定蛋白酶和腺苷合成酶A可以通过抑制保护性的Th1和Th17免疫反应,导致金葡菌的反复感染。具体来说,腺苷合成酶A通过腺苷/A2AR途径抑制NLRP3介导的IL-1β的产生,从而干扰Th17的分化和发育,进而促进金葡菌的后续感染。该研究为金葡菌反复感染提供了一个新的解释,同时也为开发金葡菌疫苗提供充分的科学依据。目前,基于该研究的金葡菌合成生物学疫苗正在开发中。
该工作获得了深圳市、广东省科学技术厅项目和中国博士后科学基金项目、深圳合成生物学创新研究院等项目的支持。

腺苷合成酶A通过抑制保护性的Th1和Th17免疫反应,而导致金葡菌的反复感染机制。