深圳先进院成功实现黑磷基水凝胶的光控原位生物矿化
近日,中国科学院深圳先进技术研究院喻学锋研究员与深圳大学邵俊东副研究员等合作,成功利用黑磷的光化学活性实现了水凝胶的光控原位生物矿化。相关论文"Photochemical Activity of Black Phosphorus for Near-Infrared Light Controlled In Situ Biomineralization"发表在国际著名学术期刊《先进科学》(Advanced Science)上,影响因子15.804。论文第一作者是邵俊东博士,通讯作者是喻学锋研究员。
近年来,二维黑磷优异的近红外光热效应、生物相容性和生物可降解性,使其在光热治疗、药物/基因递送、生物成像和生物传感器等生物医学领域中引起了广泛关注。其中,黑磷的生物可降解性是其区别于其它无机二维光热材料最重要的特性,它可以在水和氧气的作用下,降解成人体必需的磷酸盐(PO43-)。针对这一特性,研究团队揭示了黑磷的光化学活性,并研究了黑磷基水凝胶的近红外光控原位生物矿化现象和潜在用途。
磷酸盐(PO43-)和钙离子(Ca2+)的生物矿化过程在人体硬组织如牙齿和骨骼等的形成与再生过程中起到了至关重要的作用。然而在生物体内,生物矿化过程通常是自发进行的,受生物体内的生物大分子控制,很难在体外实现人为调控。然而,黑磷优异的近红外光响应特性和生物可降解性能,为实现可控的生物矿化提供了可能。研究结果显示,近红外光照不仅增强了黑磷的化学活性,促进了黑磷向磷酸盐(PO43-)转化的降解过程,还加剧了磷酸盐(PO43-)与钙离子(Ca2+)的反应过程,最终实现了可控的原位生物矿化。在此过程中,黑磷不仅是生物矿化的引发剂和调节器,还可以作为成核位点并提供生物矿化必需的磷源——磷酸盐(PO43-)。研究团队随后将黑磷与水凝胶复合,利用3D打印技术制备了骨组织工程支架,并实现了其近红外光控原位生物矿化。相关研究成果进一步拓展了黑磷的生物医学应用,并在生物材料领域,特别是组织工程中具有巨大的应用潜力。
本项研究得到了中科院前沿科学研究重点计划、广东特支计划、国家自然科学基金等项目的资助。
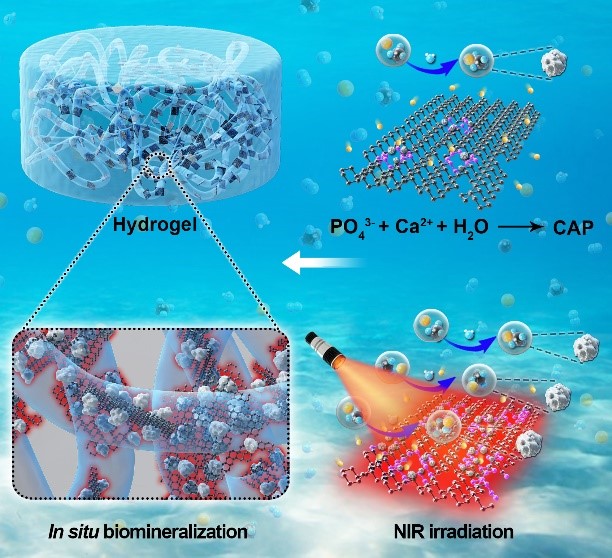
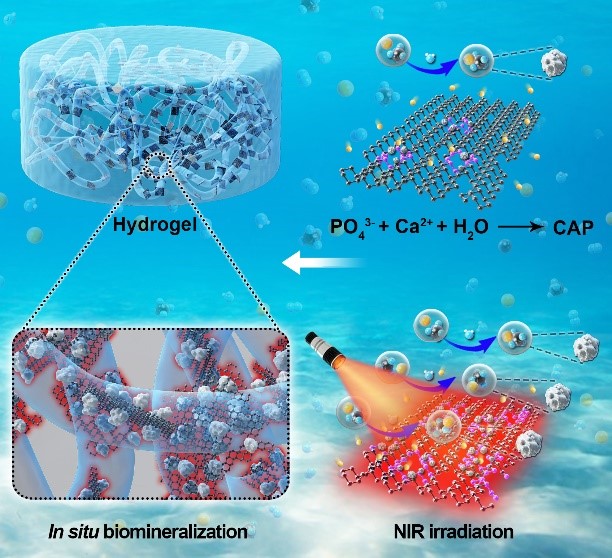
黑磷基水凝胶的光控原位生物矿化示意图