PNAS | 体内直接组装神经界面,实现局部和全身性免疫调节
北京时间11月30日,中国科学院深圳先进院脑所副研究员都展宏等展示了一种不使用聚合物载体且无需手术即可直接在组织内组装神经界面的方法,其产生的神经界面可以有效连接弥散在深层筋膜骨膜中的神经末梢。该技术能有效地通过神经刺激调节局部和全身免疫反应,为病理性异常神经活动的治疗提供了新的视角。相关成果以Doping-induced Assembly Interface for Non-Invasive in vivo Local and Systemic Immunomodulation为题发表于最新一期PNAS。
神经系统的复杂性和精细性使其成为生物学研究中最引人入胜的领域之一。在外周神经调控领域,特别是对于弥散分布在组织中的小直径神经,建立稳定的直接连接一直是一个巨大挑战。目前,除了坐骨神经等大直径外周神经,研究领域长期缺乏有效的方法来与这些神经建立稳定连接,本研究的核心在于开发了一种基于单组分多层纳米片的体内自组装系统实现这一目标。
本研究实现的纳米片包括苯磺酸根作为掺杂剂层,低氧化程度的聚3,4-乙烯二氧噻吩作为共轭层,聚多巴胺作为稳定剂和粘附剂,以及MXene作为过氧化物酶和结构核心层。该溶液体系可通过喷射注射器直接注入到特定神经末梢,利用注射过程中伴随的活性氧(ROS)催化PEDOT进一步氧化掺杂,增强纳米片间的 - 相互作用,形成导电、可生物降解的连续神经电子界面。聚多巴胺作为稳定剂,在注射前可以抑制纳米片的自发掺杂,在注射后可以与周围组织产生多种键链接,增强组装体系的体内稳定性。该神经界面不仅可以调节局部免疫活动,促进受损神经小鼠的感觉和运动神经功能恢复,而且在对清醒小鼠足三里迷走神经刺激中,激活了小鼠的迷走-肾上腺轴,从而释放儿茶酚胺类神经递质,达到抑制全身性细胞因子风暴的目的。
在体外和体内的实验中,这些纳米片在神经组织周围形成聚集,并在10周后逐步氧化代谢降解。对注射后电极阻抗的测量显示本研究形成的神经界面降低了透皮阻抗,并在刺激所用的20Hz频率上呈现出显著的下降。
在体外和体内的坐骨神经损伤相关实验中,注射后的神经组织在宏观和细胞水平上显示出积极的修复迹象,包括促进施旺细胞的生存和招募,以及促进巨噬细胞的M2极化。
这种界面能够通过激活迷走-肾上腺轴来诱导抗炎反应,而不触发脊髓交感反应,证明了其可通过神经通路的调控实现全身性免疫调节。
总而言之,这项创新的研究在神经电子学领域开辟了新的方向,为神经损伤治疗和免疫调节提供了全新的视角和策略,此类技术有望在未来的临床应用中为神经系统疾病的治疗带来更多关键突破。
深圳先进院前客座学生沙葆凝为本文第一作者,现在哥伦比亚大学继续深造,深圳理工大学(筹)生命健康学院智能交叉科学中心、深圳先进院脑所脑信息中心副研究员都展宏为本文通讯作者。本文共同作者包括合作团队PI先进院脑所所长王立平研究员、中科大和先进院脑所毕国强教授、哥伦比亚大学Dion?Khodagholy副教授,均为本文提供了重要指导和大力支持,共同作者还包括中科大纳米学院联培研究生赵生卓和课题组科研助理顾敏铃。本研究受到了科技创新2030-“脑科学与类脑研究”重大项目青年科学家项目,国家自然科学基金委重点、青年项目,科技部重点领域研发计划,广东省重点领域研发计划,中科院战略性先导科技专项,基金委-广东省联合项目,深圳市基础研究项目,深圳市脑解析与脑模拟重大科技基础设施,深港脑科学创新研究院等项目和平台的支持。团队感谢 Hao Huang 和Zhengsheng Li在材料表征等实验方面的支持和帮助。
都展宏课题组(生物电子界面工程实验室,BEIE Lab)正在积极寻求科研合作,课题组长期招聘神经生理学、生物医学工程、电化学材料等交叉学科背景方向的博士后,如有合作或加入意向,欢迎联系

图1 无需手术即可直接在体内组装的神经界面,可通过电刺激调节局部和全身免疫反应
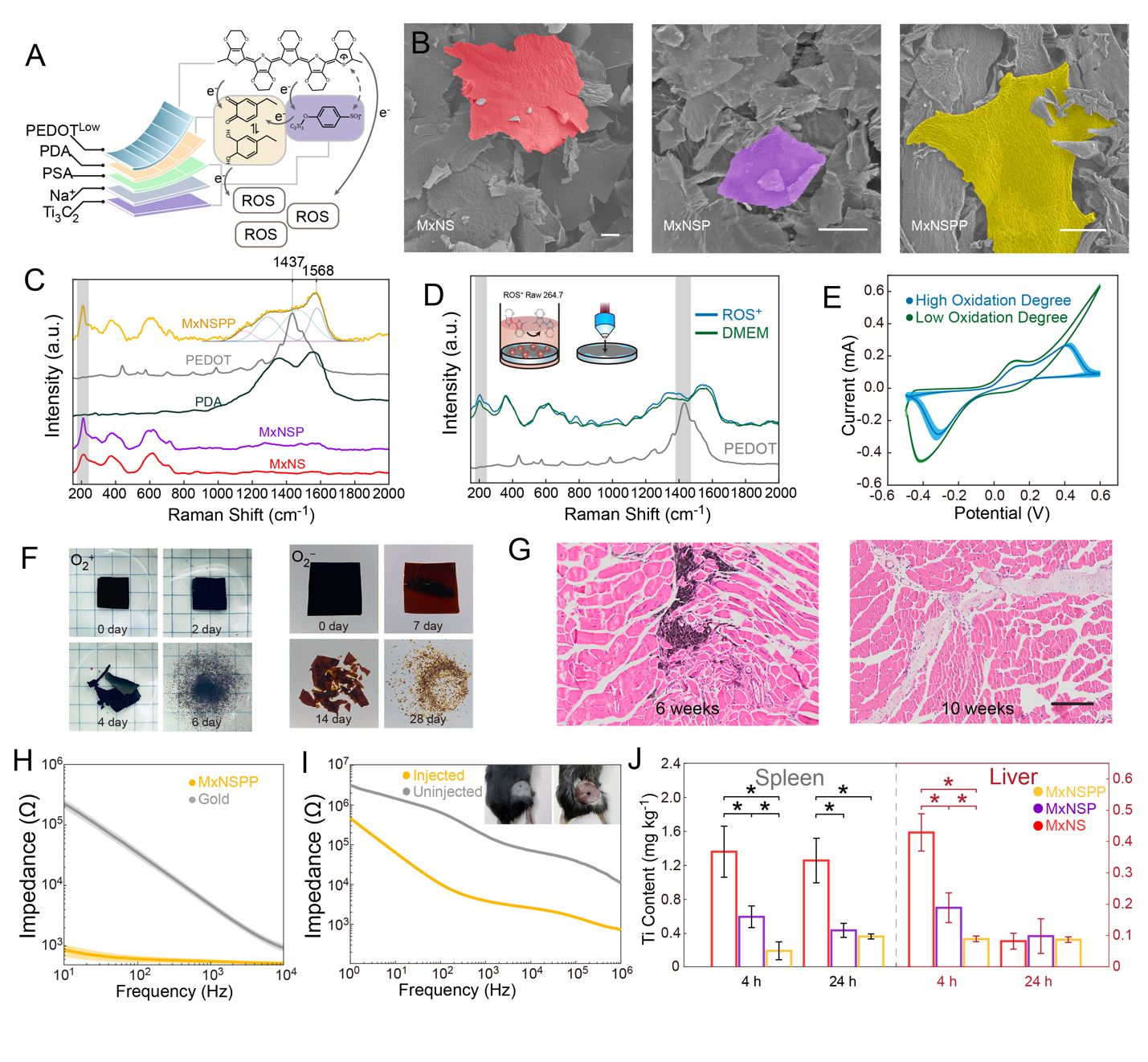
图2 本研究的二维纳米片在体内的自组装和电化学重构能力得到了验证
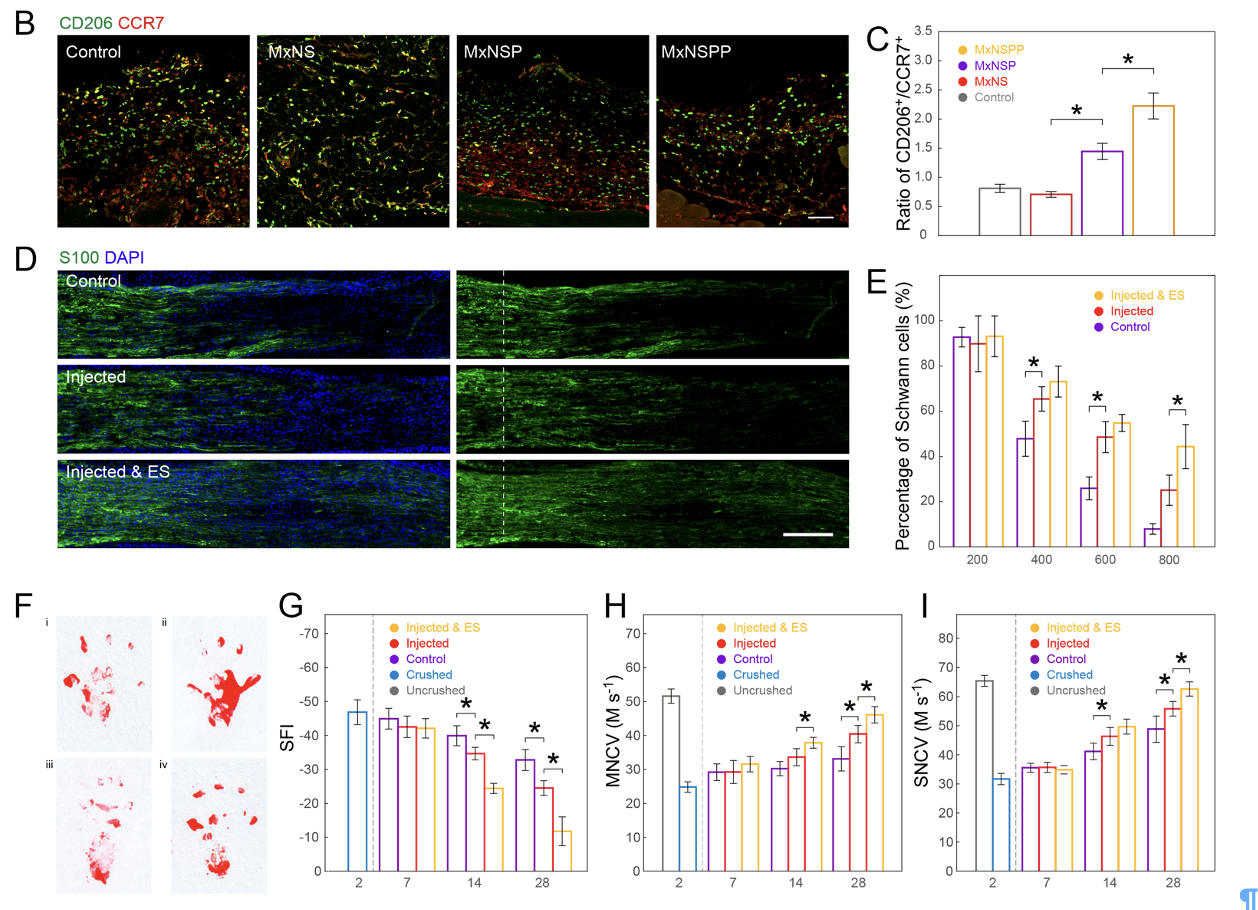
图3 研究展示了该界面在调节局部炎症反应和促进神经修复方面的潜力
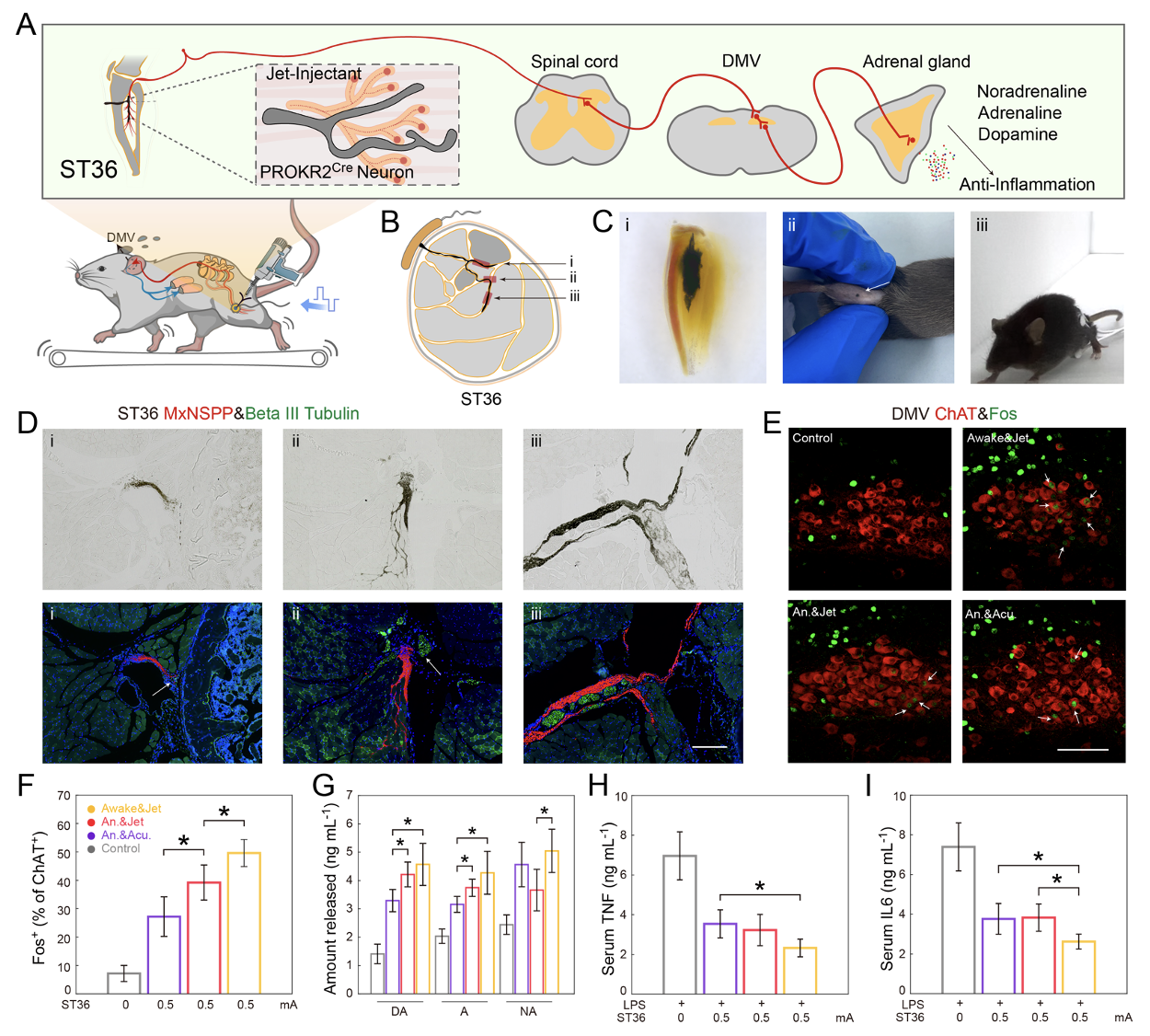
图4 研究揭示了该自组装界面在抑制全身性细胞因子释放综合征方面的潜力




